Les fondamentaux
Bien qu'elle représente un marché relativement restreint à l'échelle mondiale, l'Australie se classe parmi les principaux développeurs de MedTech dans le monde et elle occupe la 13ème place en valeur totale du marché.
Le marché des dispositifs médicaux en Australie est un marché en croissance estimé à 4,6 Mds EUR en 2023.
Les soins de santé sont fournis à la fois par les secteurs public et privé. Les politiques gouvernementales en matière de santé exercent donc une influence sur le volume et la tarification des produits et services de santé. Les dépenses combinées du gouvernement fédéral et des États représentent 70 % des dépenses totales de santé. Le secteur non gouvernemental, qui inclut les particuliers et l'assurance maladie privée, couvre les 30 % restants. Environ 55 % des Australiens disposent d'une assurance maladie privée.
Selon l’OCDE, les dépenses totales de santé en 2022 en Australie étaient estimées à 9,8 % du PIB et 6 372 USD par habitant, soit le 11ème plus élevé des 38 pays de l'OCDE. Le pays est classé au 5e rang pour la qualité de son système de santé, avec une couverture médicale universelle grâce à deux systèmes d'assurance, public et privé.
En 2023, le gouvernement australien a défini les 5 forces majeures qui façonneront l'économie australienne pour les prochaines décennies, dont le vieillissement de la population, l'utilisation accrue de la technologie numérique et des données et la demande croissante de services de soins et d'assistance.
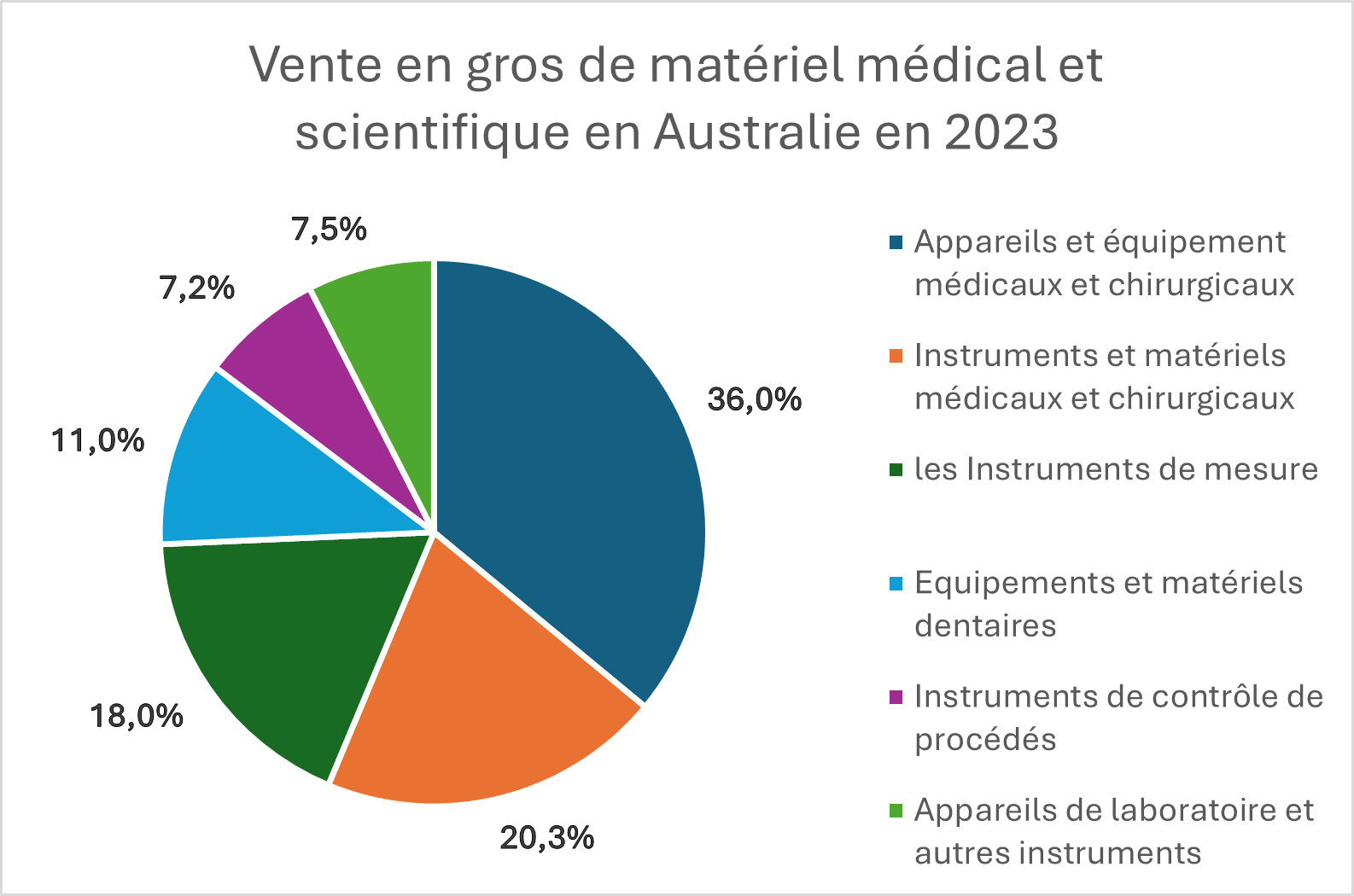
En 2023, les ventes en gros d’équipements médicaux et scientifiques ont engendré un revenu de 10,4 Mds EUR.
Vente en gros de matériel médical et scientifique en Australie en 2023
Opportunités pour l'offre française
L'Australie est une destination privilégiée pour les essais cliniques en phase I et II pour les entreprises internationales en raison de la qualité de ses recherches et ses données, de l'excellence de ses professionnels de la santé, de la rapidité des approbations réglementaires et de la stabilité de son environnement sociopolitique.
Sydney et Melbourne constituent les 2 hubs majeurs en Australie, réunissant près de 80% des entreprises de Medtech et de santé numérique.
Les maladies mentales, la démence et les maladies chroniques du foie sont parmi celles qui connaissent la croissance la plus rapide. Le nombre de maladies chroniques plus communes, telles que le diabète, les maladies cardiovasculaires, l'arthrite et l'asthme, reste élevé.
En Australie, des compensations fiscales sont allouées aux entreprises effectuant de la R&D et/ou des essais cliniques sur le territoire australien.
Les dépenses publiques dans les soins aux personnes âgées ont augmenté de 28% depuis 2018, dépassant les 17 Mds EUR en 2023.
Le Medical Research Future Fund est un fond d’investissement de 13,54 Mds EUR destiné aux maladies émergentes.
Source : Ausbiotech, Australian Institute of Health and Welfare, Australian Department of Health and Aged Care, Department of Industry Science and Resources (30/06/2024)
Responsabilité sociétale
Innovation et expertise attendues
Le marché des dispositifs médicaux est axé sur l'innovation principalement par le biais des recherches novatrices et internationales réalisées dans les universités, établissements de recherche et hôpitaux australiens. Le système de santé australien utilise depuis longtemps les nouvelles technologies (dossier médical numérique, prescription électronique, télésanté et télémédecine) pour améliorer les soins de santé.
La réglementation spécifique liée aux enjeux environnementaux
Les Australian Regulatory Guidelines for Medical Devices (ARGMD) fournissent des recommandations sur l'importation, l'exportation et la distribution de dispositifs médicaux en Australie et expliquent les exigences légales et postérieures à la mise sur le marché. L'ARGMD repose sur le système de classification basé sur le risque, qui classe les dispositifs médicaux en 4 catégories.
Les directives de l’ARGMD comprennent des exigences de sécurité et de performance appelées "Essential Principles". Tous les dispositifs doivent respecter six principes généraux qui concernent la santé et la sécurité. 9 autres principes essentiels relatifs à la conception et à la fabrication s'appliquent au cas par cas.
L'évaluation de la conformité permet de vérifier qu'un dispositif médical (y compris les dispositifs médicaux de diagnostic in vitro) répond aux « principes essentiels » de l'ARGMD.
Labels et certifications
Dans certains cas, les fabricants de dispositifs médicaux possédant un certificat CE conforme au EU Medical Devices Directive 93/42/EEC (MDD) ou EU Active Implantable Medical Devices Directive 90/385/EEC (AIMDD) peuvent utiliser cette certification pour appuyer leur enregistrement auprès du ARTG pour mettre en place un certificat TGA Conformity Assessment.
Depuis 1999, l’ARM (Accord de Reconnaissance Mutuelle) facilite le processus d’enregistrement en reconnaissant la compétence de certains organismes européens pour réaliser ces tests.
Clés d'accès
Le profil des partenaires / approche commerciale à privilégier
La réglementation australienne sur les dispositifs médicaux est l'une des plus matures et des plus pragmatiques au monde. En Australie, les dispositifs médicaux sont réglementés par la TGA.
L’approche commerciale recommandée pour s'insérer sur le marché australien est de créer un partenariat avec un agent-importateur-distributeur. Ce représentant se chargera de toutes les démarches d'enregistrement des dispositifs médicaux auprès de la TGA au nom de l'entreprise.
Le distributeur peut selon le contrat avec le client prendre à sa charge certains frais de transport et marketing. Un agent quant à lui pourra démarcher des clients finaux australien pour le compte de l’entreprise française et de ce fait permettra de créer des liens commerciaux.
La réglementation spécifique
La TGA tient un registre de tous les dispositifs médicaux approuvés pour une utilisation en Australie: l’Australian Register of Therapeutic Goods (ARTG), qui répertorie plus de 60 000 dispositifs en juillet 2024.
Le distributeur/importateur doit approcher la TGA, soit pour inscrire son produit à l’aide d’un certificat GMP (Good Manufacturing Practice), soit pour enregistrer son produit, auquel cas le produit doit subir des tests. Pour obtenir le certificat GMP, il faut démontrer que la fabrication du produit est en conformité avec les normes techniques, publiées par une autorité australienne ou internationale. De plus, il faut mettre en place un système de gestion de la qualité. Après avoir enregistré le produit dans le l’ARTG, les importateurs doivent maintenir à jour une liste de distribution, pendant 5 à 10 ans.
Niveau de taxation
Les taxes d’importation sont de 5 % de la valeur de la cargaison, auxquelles s’ajoute la GST (Goods & Services Tax - équivalent de la TVA) s’élevant à 10 %.
Certains produits et équipements médicaux sont exemptés de TVA. Il est important de vérifier l’éligibilité de chaque produit lors de son enregistrement ou en contactant l’Australian Border Force sur le site suivant : https://www.abf.gov.au/