Les fondamentaux
Le marché coréen des produits pharmaceutiques est estimé à 29 Mds EUR en 2023, en termes de production, ce qui le classe 4e en Asie-Pacifique.
En 2025, la Corée du Sud compte 3 386 projets de développement de médicaments, se plaçant 3e au monde derrière les États-Unis et la Chine.
Le pays bénéficie d’un marché intérieur solide, d’un volume d’exportation élevé, avec une concentration croissante sur la R&D. La demande est principalement en B2B, qui représente 85 % de la consommation pharmaceutique. Les importations restent limitées à 25,6 % du marché, dominé par les distributeurs locaux.
Le taux de fécondité est tombé à 0,76 %, le plus bas au monde.
Vieillissement rapide de la population : en 2024, les plus de 65 ans représentent 15,6 % de la population et ce taux atteindra 30,9 % en 2036. Combiné à une médecine centrée sur la qualité de vie, ce facteur entraîne une augmentation durable de la demande en soins chroniques, en oncologie, en neurologie et en médecine préventive. Cette dynamique soutient la croissance du secteur pharmaceutique, même dans un contexte de ralentissement économique global.
Importations de produits pharmaceutiques en Corée du Sud en 2024
Principaux pays fournisseurs
4,4 Mds EUR52 %
Reste du monde
Opportunités pour l'offre française
La Corée présente un potentiel dans les segments de l’oncologie, de la cardiologie et des neurosciences, soutenu par l’excellence hospitalière (38 établissements classés en 2024). Le pays est généralement bien classée en santé publique, mais les problématiques restent présentes : obésité, consommation d’alcool, tabagisme, vieillissement de la population, pollution atmosphérique etc..
Les opportunités dans les domaines de l’IA appliquée à la pharma, des biotechs ciblant les maladies rares, et des plateformes de R&D sont des axes où la France peut se positionner.
Le nombre de médicaments innovants introduits dans le pays a augmenté à un rythme rapide. La Corée est en train de devenir une puissance mondiale grâce à son infrastructure biotechnologique développée, ses études cliniques avancées et sa technologie informatique, mais également ses alliances stratégiques avec des multinationales.
Parmi les priorités du gouvernement dans la santé, 4 axes majeurs : protection de la vie des personnes, établissement d’une sécurité sanitaire, promotion des nouvelles industries biosimilaires, création d’un écosystème innovant R&D.
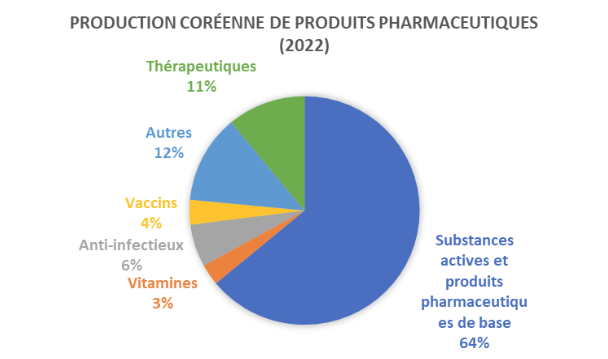
Source : KOFICE, OCDE, GTA Connect, Euromonitor, Presse locale (11/08/2025)
Responsabilité sociétale
Innovation et expertise attendues
Le secteur mise résolument sur l’innovation, portée par la convergence entre biotechnologie, IA, médecine personnalisée et robotique médicale.
L’expertise étrangère est particulièrement recherchée dans les domaines des thérapies avancées (cellulaires, géniques, ADC), du diagnostic de précision, de la formulation sous-cutanée, et de la bioproduction conforme aux standards GMP internationaux.
L’IA est désormais intégrée dans les processus de découverte de médicaments, permettant de réduire les coûts de développement de plus de 65 % et les délais de mise sur le marché de 10 ans à 2 ans.
Les entreprises coréennes s’ouvrent à des partenariats technologiques pour accélérer l’accès à des plateformes innovantes, notamment dans les domaines de l’édition génomique, des vaccins personnalisés, et des modèles prédictifs de réponse immunitaire.
Clés d'accès
Le profil des partenaires / approche commerciale à privilégier
Dans un secteur très régulé, les fabricants de produits pharmaceutiques doivent obligatoirement passer par un grossiste pour pouvoir vendre des médicaments sur ordonnance en Corée du Sud.
Pour les médicaments en libre accès (OTC) en revanche, il est possible de faire appel à un grossiste ou bien de négocier directement avec les pharmacies et les établissements de santé.
Bien que l’écart se resserre, la Corée du Sud est toujours, sur certains segments, en retard sur la R&D par rapport à des groupes ou biotech occidentales : les groupes pharmaceutiques coréens sont favorables à des contrats de « licensing-in/out » avec les entreprises étrangères, ou des contrats de CRO (CDMO dans une moindre mesure).
La réglementation spécifique
La commercialisation des dispositifs médicaux en Corée est règlementée par le Ministry of Food and Drug Safety (MFDS) selon le Medical Device Act. Le certificat KGMP (Korean Good Manufacturing Practices) est un prérequis à tout enregistrement et doit être renouvelé tous les 3 ans.
Les produits pharmaceutiques en Corée du Sud sont régulés par le Ministry of Food and Drugs Safety (MFDS) selon deux textes de références que sont le « Pharmaceutical Act » et le « Regulation on Safety of Pharmaceuticals ».
Le « Pharmaceutical Act » établit 2 types de produits pharmaceutiques : d’une part, les ingrédients pharmaceutiques et d’autre part, les médicaments nouveaux, biologiques, génériques ou orphelins. La procédure d’enregistrement et les délais varient en fonction de la classification du produit.
Niveau de taxation
En vertu de l’accord de libre-échange Corée-UE, la quasi-totalité des droits de douanes sur les produits pharmaceutiques importés en Corée du Sud ont été supprimés.
Le taux de TVA est fixé à 10 %.
Le French Healthcare Korea Club (FHK) œuvre à la coordination des actions dans le secteur de la santé, tout en favorisant les synergies entre l'écosystème français et coréen. Le FHK assure la promotion de l'excellence de la santé française en Corée du Sud.

Source : MFDS, Douanes coréennes (11/08/2025)








